(
الإلكترون (
بالإنجليزية: Electron) هو
جسيم دون ذري مكون
للذرة ويحمل
شحنة كهربائية سالبة. ولم يكن من المعروف بأن لديها مكونات أو جسيمات أصغر، لذا فقد اعتبرت بأنها
جسيمات أولية[2]. فالإلكترون لديه
كتلة تعادل تقريبا 1/1836 من كتلة
البروتون[8].
الزخم الزاوي الحقيقي (وهو
اللف المغزلي) للإلكترون هو قيمة نصف عدد صحيح من وحدة
ħ، مما يعني بأنه
فرميون. ويسمى
الجسيم المضاد للإلكترون
بالبوزيترون، وهو مطابق للإلكترون عدا أنه معاكس له بالشحنة الكهربائية
والشحنات الأخرى. عند اصطدام الإلكترون بالبوزترون فإنهما إما يبعثرون بعضهم البعض أو أن
يفنون، مما ينتج عن ذلك زوج أو أكثر من
فوتونات أشعة جاما. تنتمي الإلكترونات إلى
الجيل الأول لأسرة جسيمات
ليبتون[9]، وتسهم في
القوى الأساسية وهي
الجاذبية والكهرومغناطيسية وقوى نوويية ضعيفة[10]. كما هو في المادة فإن الإلكترون لديه خصائص
ازدواجية موجة-جسيم في
ميكانيكا الكم، لذا فبإمكانه الإصطدام مع الجسيمات الأخرى
فينحرف مثل الضوء. لكن وبسبب صغر كتلة الإلكترون فإن تلك الإزدواجية تتجلى بشكل أفضل في التجارب المخبرية. وبما أنها تندرج تحت عائلة الفرميون، وبحسب
مبدأ استبعاد باولي فلا يمكن لإلكترونين أن يأخذا نفس حالة الكم
[9].تم وضع نظرية مفهوم مقدار الشحنة الإلكترونية غير القابلة للتجزئة لشرح
الخصائص الكيميائية للذرات، فكانت بدايتها سنة 1838 مع عالم الطبيعة البريطاني
ريتشارد لامنج[4]؛ ثم قدم الفيزيائي الإيرلندي
جورج ستوني (en) اسم
الكترون وذلك سنة 1894. في سنة 1897 عرّف البريطاني
جوزيف طومسون وفريقه الفيزيائيين الإلكترون بأنه جسيم
[6][11].العديد من الظواهر الفيزيائية، مثل
الكهرباء والمغناطيسية والتوصيل الحراري فإن الإلكترونات لها دورا أساسيا في ذلك. فالإلكترون في حركته بالنسبة للمراقب يولد
المجال المغناطيسي، وكذلك فإن المجالات المغناطيسية الخارجية تجعلها تنحرف. فعندما يتحرك الإلكترون فإنه يمتص أو ينتج طاقة على شكل فوتونات. تحيط الإلكترونات
بالنواة المتكونة من
بروتونات ونيوترونات، فيكونون جميعا الذرة، وإن كان الإلكترون يسهم في أقل من 0.06% من الكتلة الكلية للذرة. يسبب جاذبية
قوة كولومب بين الإلكترون والبروتون بأن يجعل الإلكترونات
مرتبطة بالذرات. فالتبادل أو تقاسم الإلكترونات في ما بين الذرات هو السبب الرئيسي
للروابط الكيميائية[12].فحسب النظريات فإن معظم إلكترونات قد تكونت في لحظة
الإنفجار العظيم، ولكن يمكن أيضا إنتاجها خلال
البلى بيتائي للنظائر المشعة والإصطدامات عالية الطاقة، وفي لحظة دخول
الأشعة الكونية للغلاف الجوي. وخلال إفناءه مع البوزترون فقد يتعرض الإلكترون للدمار، وقد يتعرض للإمتصاص خلال
تفاعلات الإنصهار النجمية. ويمكن لأدوات المختبرات احتواء ومراقبة الإلكترونات الفردية وكذلك في
بلازما الإلكترونات، حيث كرس لها
المقراب للكشف عن بلازما الإلكترونات في الفضاء الخارجي. وتوجد العديد من تطبيقات الإلكترون كما هو في
اللحام وأنبوب الأشعة المهبطية ومعجلات الجسيمات ومجهر إلكتروني وعلاج إشعاعي وليزر الكتروني (en).//
التاريخلاحظ
الإغريق القدماء بأن
الكهرمان يجذب الأشياء البسيطة في حالة فركه بالفرو؛ فإن استثنينا
البرق، فإن تلك الظاهرة تعد من أقدم تجارب البشرية مع الكهرباء على مر التاريخ
[13].أشار الفيزيائي الإنجليزي
وليام جيلبرت في مقال له اسمه دي ماجنتا
De Magnete سنة 1600 إلى مصطلح جديد أصاغه من اللغة
اللاتينية الجديدة وأسماه إلكتريكوس
electricus للإشارة إلى خاصية جذب الأشياء الصغيرة بعد فركها
[14]. فتلك الكلمة مأخوذة من الكلمة الإغريقية ήλεκτρον (
ēlektron)
الكترون في عام
1894 م للإشارة إلى الكهرمان.في سنة 1737 اكتشف العالمين
شارل دو فاي وهوكسبي كلا على حدة وجود نمطين من الشحنات الكهربائية السكونية؛ إحداهما ينتج من الإحتكاك مع الزجاج، والآخر من الإحتكاك مع
الراتنج. ومن هذه استنتج دوفاي نظريته بأن الكهرباء تحتوي على
سائلين كهربائيين (en)، وأسماهما بالزجاجي والراتنجي، ولاحظ الفرق بين الموصلات والمواد العازلة، ويمكن فصلهما عن طريق الاحتكاك مما يسبب بتحييد بعضها البعض عند اتحادهما
[15]. بعد ذلك بحوالي عقد من الزمان اقترح
بنجامين فرانكلين بأن الكهرباء هي ليست من عدة أنواع من السوائل الكهربائية، ولكنه نفس السائل الكهربائي ولكن تحت ضغوط مختلفة. وقدم لهم
الشحنة الحديثة بتسمية إيجابي وسلبي على التوالي
[16][17].بين سنتي 1838 و 1851 طور عالم الطبيعيات البريطاني
ريتشارد لامنج} فكرة أن الذرة تتكون من نواة مادة محاطة بجزيئات دون ذرية والتي تكوّن وحدة
الشحنات الكهربائية[3]. وبداية من سنة 1846 أعطى الفيزيائي الألماني
فيبر نظريته القائلة بأن الكهرباء تتألف من سائلين ذو شحنتين موجبة وسالبة، وتفاعلهما يحكمه
قانون التربيع العكسي (en). في سنة 1874 اقترح الفيزيائي الإيرلندي
جورج ستوني بعد دراسة هذه ظاهرة
التحليل الكهربائي بأن هناك "كمية محددة واحدة من الكهرباء" ، وهي شحنة من
أيون أحادي التكافؤ. وكان قادرا على تقييم قيمة هذه الشحنة الأولية
e عن طريق
قوانين فرداي للتحليل الكهربائي[18]. واعتقد ستوني بأن تلك الشحنات مرتبطة بصورة دائمة بالذرات ولا يمكن إزالتها. في سنة 1881 جادل الفيزيائي الألماني
هلمهولتز أن كلا من الشحنة الموجبة والسالبة منقسمتين إلى جزئين أوليين، كل منها "يتصرف كذرات كهربائية"
[4]. ثم أنشأ ستوني مصطلح
الكترون لوصف تلك الشحنات الأولية وكان ذلك سنة 1894، وقد قال فيها: "تم تقدير الكمية الفعلية لتلك الوحدة الأساسية الأكثر أهمية في الكهرباء، وقد غامرت عندما أشرت إلى اسم
الكترون"
[19]. وكلمة الكترون (
بالإنجليزية: electron) هي مركبة مستنبطة من كلمة الكتريك
electric ولاحقتها ون
-on، والتي استخدمت بعد ذلك للإشارة إلى
الجسيمات دون الذرية مثل البروتون والنيوترون
[20][21].
الإكتشاف

انعكاس شعاع من الإلكترونات على شكل دائرة بواسطة المجال المغناطيسي
[22]قام الفيزيائي الألماني
يوهان ويلهلم هيتورف (en) بدراسة التوصيل الكهربائي على الغازات المتخلخلة. فاكتشف سنة 1869 وهج منبعث من
مهبط يزداد بالحجم عند تقليل ضغط الغاز. وفي سنة 1876 أظهر الفيزيائي الألماني
يوجين غولدشتاين (en) أن أشعة هذا الوهج له ظل، فأطلق عليه اسم لهم
أشعة الكاثود[23]. وفي السبعينات من نفس القرن طور الكيميائي والفيزيائي الإنجليزي
السير وليام كروكس (en) أول أنبوب أشعة الكاثود
مفرغة بالداخل
[24]. ثم أظهر بعد ذلك بأن أشعة التلألؤ التي تظهر داخل أنبوب تحمل طاقة وتنتقل من القطب السالب إلى
القطب الموجب. بالإضافة إلى أنه كان قادرا على تحريك الأشعة عند تطبيق مجال مغناطيسي عليها، مما يدل على أن الشعاع تصرف كما لو كان سالب الشحنة
[25][26]. فاقترح سنة 1879 أنه بالإمكان تفسير تلك الخصائص من خلال مااسماه مادة مشعة. وألمح إلى أن قد تكون هذه الحالة الرابعة للمادة التي تتكون من
جزيئات سالبة الشحنة تنطلق بسرعة عالية من الكاثود
[27].وسع الفيزيائي البريطاني -ألماني المولد-
آرثر شوستر من تجارب كروكس وذلك بوضع صفيحة معدنية متوازية مع أشعة الكاثود وطبق
الكمون الكهربائي بين الصفيحتين. فصرف المجال تلك الأشعة باتجاه الصفيحة موجبة الشحنة، مما أعطى أدلة جديدة على أن تلك الأشعة تحمل شحنة سالبة. وتمكن شوستر في سنة 1890 من تقدير
نسبة الشحنة للكتلة لمكونات الأشعة عن طريق قياس مقدار انحراف عن المستوى المحدد
للتيار. لكن أنتاج تلك القيمة التي كانت أكثر من ألف مرة من المتوقع، هو إعطاء بعض المصداقية لتلك الحسابات في ذاك الوقت
[25][28].في عام 1896 أجرى الفيزيائي البريطاني
جوزيف طومسون مع مساعديه تاونسند وويلسون
[6] تجارب أشارت إلى أن أشعاعات الكاثود هي جسيمات فريدة من نوعها بدلا من أن تكون موجات أو ذرات أو حتى جزيئات كما كان الإعتقاد سابقا
[29]. وقد أعطى طومسون قيمة جيدة لكل من الشحنة
e والكتلة
m، موجدا جسيمات ل
أشعة الكاثود واسماها "الكريات" (
بالإنجليزية: corpuscles)، ولها كتلة قد تكون واحد من الألف من كتلة أقل الأيونات المعروفة: الهيدروجين
[11][29]. وأظهر أن نسبة الشحنة للكتلة
e/
m مستقلة عن مادة الكاثود. وأظهر أيضا أن إنتاج جسيمات سالبة الشحنة من مواد مشعة بواسطة التسخين ومن مواد مضيئة هو شيء كوني
[29][30]. وقد أعاد الفيزيائي الأيرلندي جورج فيتزجيرالد الإقتراح بتسمية تلك الجسيمات باسم إلكترون، وقد لقي هذا الاسم قبولا علميا دوليا منذ ذلك الوقت
[25].اكتشف الفيزيائي الفرنسي
هنري بيكريل أثناء دراسة
الومضان الطبيعي للمعادن سنة 1896 أنها تصدر إشعاع دون التعرض لمصدر طاقة خارجي. فأصبحت تلك
المواد المشعة موضع اهتمام كبير للعلماء خصوصا الفيزيائي
النيوزلندي إرنست رذرفورد الذي اكتشف أنها تصدر جسيمات. وأطلق عليها
جسيمات ألفا و
بيتا على أساس قدرتها على اختراق المادة
[31]. وفي سنة 1900 أظهر بيكريل أن بإمكان أشعة بيتا المنبعثة من
الراديوم أن تنحرف في وجود مجال كهربائي وأن نسبة الكتلة للشحنة هي نفسها كما في أشعة الكاثود
[32]. فعززت هذا الدليل الرأي القائل بأن الالكترونات توجد كعناصر في الذرات
[33][34].قام الفيزيائي الأمريكي
روبرت ميليكان بعناية ودقة أكثر في قياس شحنة الإلكترون في
تجربة قطرة الزيت سنة 1909 ثم نشر النتائج سنة 1911. واستخدمت تلك التجربة المجال الكهربائي لمنع قطرات الزيت المشحونة من السقوط بسبب الجاذبية. وامكن لهذا الجهاز قياس الشحنة الكهربائية حتى 1-150 أيون مع هامش خطأ اقل من 0.3٪. وقد أجرى فريق طومسون تجارب مماثلة قبل ذلك
[29]، باستخدام سحب من قطرات الماء المشحونة انتجها التحليل الكهربائي
[6]. وقد حصل
ابرام عيوفي (en) بشكل منفصل على نفس نتائج ميليكان وذلك باستخدام جسيمات مجهرية من المعادن، وكان ذلك سنة 1911 ولكن نشر النتائج سنة 1913
[35]. مع ذلك فإن قطرات الزيت أكثر ثباتا من قطرات الماء بسبب ضعف معدل التبخير لديه، وبالتالي فالتجارب الدقيقة بدأت أكثر ملاءمة خلال فترات زمنية أطول
[36].وجد عند بداية القرن العشرين وفي ظروف معينة جسيمات مشحونة سريعة الحركة تسبب بتكثيف بخار ماء
مفرط بالتشبع (en) خلال مساره. ففي سنة 1911 استخدم
تشارلز ويلسون هذا المبدأ لاستنباط
غرفة الغيوم مما يسمح بتصوير مسارات الجسيمات المشحونة مثل الإلكترونات سريعة الحركة
[37].
النظرية الذرية
 نموذج بور للذرة
نموذج بور للذرة والتي يبين حالات من الكترون ذات طاقة
كم محددة بالرقم n. فعندما ينتقل الإلكترون إلى مدار أدنى فإنه ينبعث منه طاقة فوتون تساوي الفرق بين طاقة المدارين.
شكلت التجارب التي قام بها كلا من أرنست رذرفورد و
هنري موزلي و
جيمس فرانك و
غوستاف هرتس بداية من سنة 1914 الصورة في تكوين الذرة
كنواة كثيفة ذات شحنة موجبة تحيط بها إلكترونات أقل كتلة
[38]. ثم أتى الفيزيائي الدانماركي
نيلز بور فافترض في سنة 1913 بأن الالكترونات تكمن في حالات طاقة كمية، ويحدد العزم الزاوي لمدار الإلكترون حول النواة تلك الطاقة. وبإمكان تلك الإلكترونات التنقل بين تلك الحالات أو المدارات عن طريق إطلاق أو امتصاص فوتونات ذات ترددات محددة. ومن خلال تلك المدارات محددة الكم أوضح نيبور بدقة
خطوط الطيف لذرة الهيدروجين
[39].ومع ذلك ف
نموذج بور لم يتمكن من تفسير الفروق في الكثافة النسبية لخطوط الطيف، وكذلك أطياف العناصر الأثقل من الهيدروجين، فهي بالكاد اقتصرت على تفسير ذرة
الهيدروجين[38].وقد شرح
جيلبرت نيوتن لويس (en) الروابط الكيميائية بين الذرات وذلك في سنة 1916 عندما اقترح بأن مساهمة زوج أو أكثر من الإلكترونات بين الذرات للمحافظة على
الرابطة التساهمية في ما بين تلك الذرات، مما ينتج عنه تجاذب جانبي يعمل على تماسك الجزيء الناتج
[40]. وبعدها أي في سنة 1923 أعطى كلا من
والتر هيتلر (en) و
فريتز لندن (en) شرحا وافيا حول تشكيل زوج الإلكترون مع الروابط الكيميائية في مجال
ميكانيكا الكم[41]. وفي سنة 1919 فصّل الكيميائي الأمريكي
إرفينغ لانغموير نموذج لويس للذرة مشيرا بأن جميع الإلكترونات موزعة على التوالي مكونة قشرة كروية متحدة المركز وذات سماكة متساوية
[42]. وتنقسم تلك القشور بدورها إلى عدة خلايا، وكل خلية تحتوي على زوج من الإلكترونات. وعلى نحو ما فإن لنموذج لانغموير القدرة على شرح
الخصائص الكيميائية لجميع العناصر في الجدول الدوري
[41]، التي كانت معروفة بتكرار نفسها وفقا
للقانون الدوري[43].لاحظ الفيزيائي النمساوي
فولفغانغ باولي في سنة 1924 بأنه يمكن تفسير البناء شبيه القشرة للذرة من خلال مجموعة من أربع معاملات متغيرة تحدد كل حالة طاقة الكم، شريطة أن يكون أن لا يزيد في كل حالة عن إلكترون واحد. (ويعرف هذا الحظر المفروض على أكثر من إلكترون أن يشغل نفس حالة كمية الطاقة باسم
مبدأ استبعاد باولي[44].) وقدم الفيزيائيان الهولنديان
ابراهام جودسميث (en) و
جورج أهلينبك (en) الآلية المادية لشرح المعامل الرابع والذي له قيمتين مميزتين، عندما اقترحوا أن بإمكان الإلكترون مع الزخم الزاوي لمداره أن يمتلك قوة زخم زاوي فعلي
[38][45]. وعرفت تلك الخاصية
باللف المغزلي وقد شرحت تقسيم سابق كان غامضا عن خطوط الطيف رصدها
مرسمة طيف عالي الدقة، وعرفت تلك الظاهرة باسم تقسيم
هيكلي دقيق (en)[46].
ميكانيكا الكمفي عام
1924 كتب الفيزيائي الفرنسي
لويس دي بروي رسالة دكتوراه بعنوان "بحث حول نظرية الكم" Recherches sur la théorie des quanta، وافترض فيها أن كل الموادّ تمتلك "
موجة دي بروي" مشابهة
للضوء.
[47] حيث أنه وتحت ظروف مناسبة ستُظهر الإلكترونات والمواد الأخرى خصائص كل من الجسيمات والضوء. ويُستدل على الخصائص الجسيميّة لجسيم ما عندما يُظهر أنه يملك موقعًا متمركزاً في
المكان يعتمد على انحناء مساره أثناء حركته.
[48] أما الطبيعة الشبه الموجية للجسيم فيُمكن أن تلاحظ - على سبيل المثال - عندما يمر شعاع من الضوء عبر شقوق متوازية ويخلق نمطاً
متداخلاً من الأشعة. في عام
1927 بُرهن على تأثير التداخل بتجرتين مختلفتين استعين فيهما بشعاع من الإلكترونات، الأولى قام بها الفيزيائي الإنكليزي
جورج باغت طومسون باستخدام رقاقة حديدية نحيلة مع الشعاع، والثانية قام بها الفيزيائيان الأمريكيان
كلنتون دافيوسين و
لستر جيرمر باستخدام بلورة من
النيكل معه.
[49]

في ميكانيكا الكم يوصف
المدار الذري سلوك الإلكترون في الذرة، وهو توزيع الإحتمالات بدلا من المدار. ويشير النطاق المظلل في الرسم إلى الاحتمال النسبي "للعثور" على الإلكترون ذو طاقة معطاة حسب
الرقم الكمي عند تلك النقطة.
أدى نجاح فرضية دي بروي ب
إرفين شرودنغر أن يصدر كتابه سنة 1926 والذي نجح أيضا في وصف كيفية انتشار موجات الإلكترونات خلال معادلته المسماة
معادلة شرودنغر[50]. وبدلا من الرضوخ إلى حل يحدد موقع الإلكترون مع مرور الوقت، فإنه بالإمكان استخدام تلك المعادلة الموجية للإفتراض باحتمالية العثور على إلكترون قريب من الموقع. سمي هذا التقريب لاحقا باسم
ميكانيكا الكم، التي اعطت اشتقاق قريب جدا لحالات طاقة الإلكترون في ذرة الهيدروجين
[51]. فعندما يؤخذ بعين الاعتبار لف وتفاعل الإلكترونات المتعددة، فإن ميكانيكا الكم يمكنها بسهولة إفتراض بترتيب إلكترونات الذرات ذات رقم ذري أعلى من الهيدروجين
[52].في سنة 1928 وبناء على مبدأ ولفغانغ باولي فقد أنتج
بول ديراك نموذجا للإلكترون وهي
معادلة ديراك وتتفق مع
مبدأ النسبية وذلك بتطبيق الاعتبارات النسبية والتماثل في صياغة
هاميلتونية (en) لميكانيكا الكم في المجال الكهرومغناطيسي
[53]. ولكي يحل بعض المشاكل داخل معادلته النسبية فقد طور ديراك نموذجا للفراغ وذلك سنة 1930 ووصفه بأنه بحر من الجسيمات ذات طاقة سلبية لانهاية لها، وقد اطلق عليها اسم
بحر ديراك. وكان هذا أدى به ذلك إلى الإفتراض بوجود جسيمات
البوزيترون، وهي
المادة المضادة النظيرة للإلكترون
[54]. تلك الجسيمات قد اكتشفها
كارل أندرسون سنة 1932، الذي اقترح بتسميتها الإلكترونات القياسية أو نيجاترون
negatrons، حيث أنها مزيج من كلمتي الكترون
electron وسلبي
negative. ولا يزال مصطلح نيجاترون يستخدم من حين لآخر، ويمكن اختصارها إلى نيجاتون 'negaton'
[55][56].وفي سنة 1947 وجد
ويليس لامب وبمساعدة أحد طلبته اسمه روبرت روثرفورد أن هناك فارق في حالات الكم لذرة الهيدروجين والتي من المفترض أن يكون لها نفس الطاقة والتي تغيرت حسب الرابطة التي بينهم، وسمي هذا الفرق ب
انتقال لامب (en). وفي نفس الفترة تلك اكتشف
كوش مع هنري فولي أن العزم المغناطيسي للإلكترون أعلى بقليل مما تنبأت به نظرية ديراك. وسمي هذا الفارق البسيط لاحقا باسم
العزم المغناطيسي الشاذ (en) للإلكترون. ولحل تلك الإشكالات طور كلا من
سين توموناجا و
ريتشارد فاينمان و
جوليان شفينجر في أواخر الأربعينيات تلك النظرية المنقحة والمسماة
كهروديناميكا الكم.
[57].
معجلات الجسيماتمع تطور
معجل الجسيمات خلال النصف الأول من القرن العشرين، بدأ الفيزيائيون في الخوض وبعمق في خصائص
الجسيمات دون الذرية[58]. وأول محاولة ناجحة لتسريع الالكترونات باستخدام
الحث الكهرومغناطيسي كانت عن طريق جهاز
بيتاترون الذي أنشأه
دونالد كريست سنة 1942. ووصلت طاقته الأولية حوالي MeV 2.3 في حين وصلت طاقة البيتاترون التالية إلى MeV 300. ثم اكتشف
الإشعاع السنكروتروني سنة 1947 بطاقة MeV 70 في شركة
جنرال إلكتريك. وكانت عملية تسريع الإلكترونات والتي قاربت سرعتها من سرعة الضوء خلال مجال مغناطيسي هي السبب في ظهور هذا الإشعاع
[59].وفي سنة 1968 بدأ العمل
بأدون وهو أول
مصادم جسيمات ذو شعاع طاقة عالي تساوي GeV 1.5
[60]. وهو أداة لتسريع الإلكترونات والبوزيترونات بإتجاهين متضادين، وذلك لمضاعفة الطاقة الفعالة من اصطدامهما عند مقارنة ضرب إلكترون بهدف ثابت
[61]. وخلال الفترة من 1989-2000 أعطى
مصادم الكترون-بوزيترون الكبير (en) (LEP) في
سرن طاقة شعاع GeV 209 وصنع قياسات مهمة
للنموذج القياسي لفيزياء الجسيمات
[62][63].
خصائص الإلكترونالتصنيف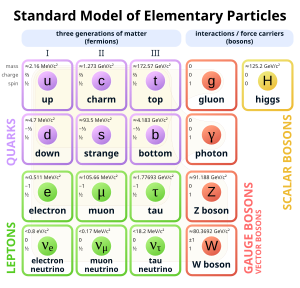

النموذج القياسي للجسيمات الأولية. الإلكترون في أسفل اليسار.
تنتمي الإلكترونات في النموذج القياسي لفيزياء الجسيمات إل

